《2018年秋九年級(jí)化學(xué)上冊(cè) 第二單元 我們周圍的空氣易錯(cuò)強(qiáng)化練 (新版)新人教版》由會(huì)員分享��,可在線閱讀���,更多相關(guān)《2018年秋九年級(jí)化學(xué)上冊(cè) 第二單元 我們周圍的空氣易錯(cuò)強(qiáng)化練 (新版)新人教版(4頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索�。
1��、
我們周圍的空氣
單元易錯(cuò)強(qiáng)化練
易錯(cuò)點(diǎn)1 空氣中氧氣含量的測(cè)定
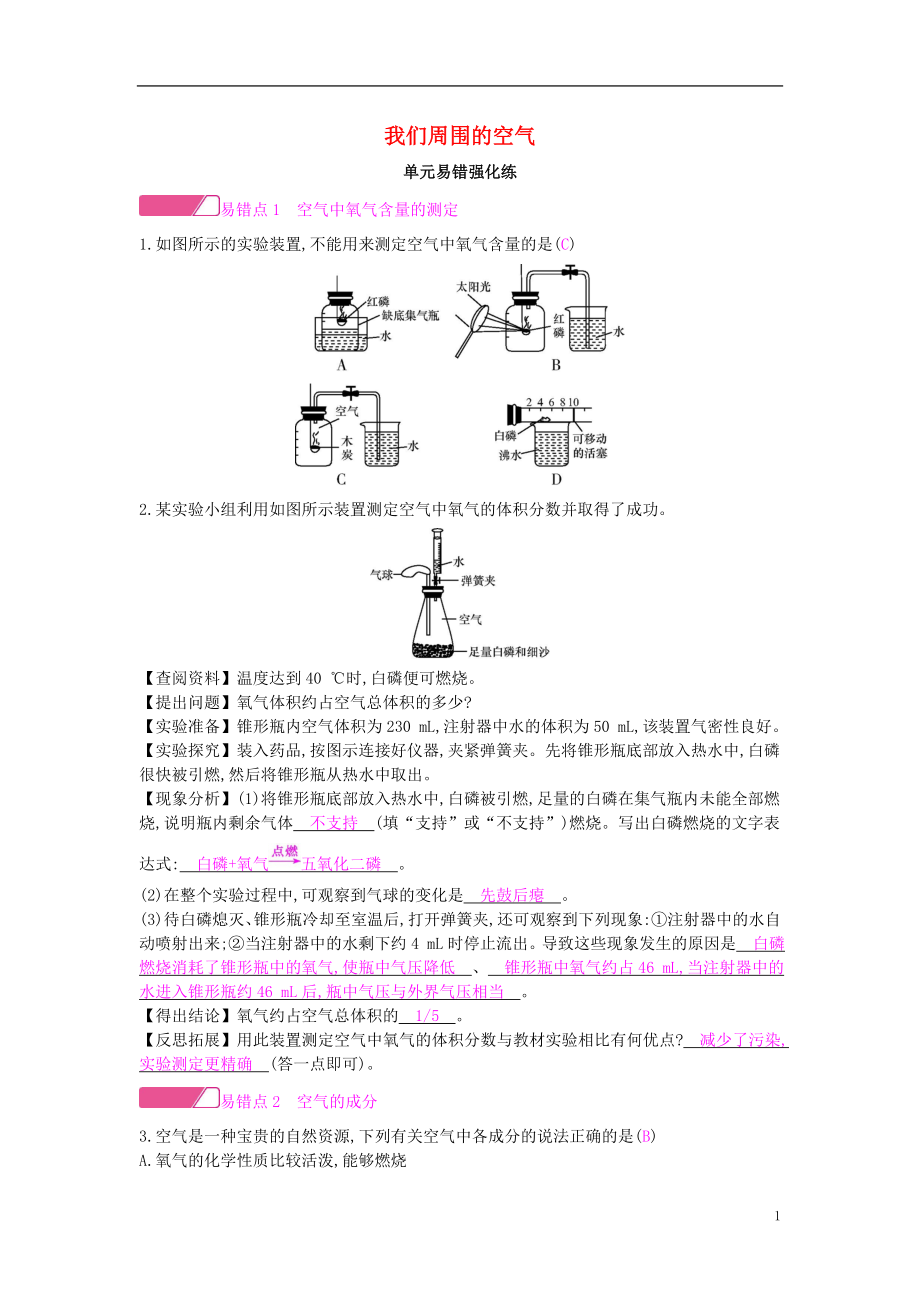
1.如圖所示的實(shí)驗(yàn)裝置,不能用來(lái)測(cè)定空氣中氧氣含量的是(C)
2.某實(shí)驗(yàn)小組利用如圖所示裝置測(cè)定空氣中氧氣的體積分?jǐn)?shù)并取得了成功�。
【查閱資料】溫度達(dá)到40 ℃時(shí),白磷便可燃燒。
【提出問(wèn)題】氧氣體積約占空氣總體積的多少?
【實(shí)驗(yàn)準(zhǔn)備】錐形瓶?jī)?nèi)空氣體積為230 mL,注射器中水的體積為50 mL,該裝置氣密性良好����。
【實(shí)驗(yàn)探究】裝入藥品,按圖示連接好儀器,夾緊彈簧夾。先將錐形瓶底部放入熱水中,白磷很快被引燃,然后將錐形瓶從熱水中取出��。
【現(xiàn)象分析】(1)將錐形瓶底部放入熱水中,白磷被引燃,足量的白磷在
2���、集氣瓶?jī)?nèi)未能全部燃燒,說(shuō)明瓶?jī)?nèi)剩余氣體 不支持 (填“支持”或“不支持”)燃燒�。寫出白磷燃燒的文字表達(dá)式: 白磷+氧氣五氧化二磷 �����。?
(2)在整個(gè)實(shí)驗(yàn)過(guò)程中,可觀察到氣球的變化是 先鼓后癟 ��。?
(3)待白磷熄滅�、錐形瓶冷卻至室溫后,打開彈簧夾,還可觀察到下列現(xiàn)象:①注射器中的水自動(dòng)噴射出來(lái);②當(dāng)注射器中的水剩下約4 mL時(shí)停止流出。導(dǎo)致這些現(xiàn)象發(fā)生的原因是 白磷燃燒消耗了錐形瓶中的氧氣,使瓶中氣壓降低 �����、 錐形瓶中氧氣約占46 mL,當(dāng)注射器中的水進(jìn)入錐形瓶約46 mL后,瓶中氣壓與外界氣壓相當(dāng) �����。?
【得出結(jié)論】氧氣約占空氣總體積的 1/5 ����。?
【反思拓展】用此裝置測(cè)定空氣中氧
3、氣的體積分?jǐn)?shù)與教材實(shí)驗(yàn)相比有何優(yōu)點(diǎn)? 減少了污染,實(shí)驗(yàn)測(cè)定更精確 (答一點(diǎn)即可)��。?
易錯(cuò)點(diǎn)2 空氣的成分
3.空氣是一種寶貴的自然資源,下列有關(guān)空氣中各成分的說(shuō)法正確的是(B)
A.氧氣的化學(xué)性質(zhì)比較活潑,能夠燃燒
B.氮?dú)獾幕瘜W(xué)性質(zhì)不活潑,可用于食品防腐
C.稀有氣體都不能與其他物質(zhì)發(fā)生化學(xué)反應(yīng)
D.二氧化碳在空氣中含量增多會(huì)引起溫室效應(yīng),屬于空氣污染物
易錯(cuò)點(diǎn)3 純凈物和混合物的判別
4.以下物質(zhì):①氮?dú)?②人體呼出的氣體;③稀有氣體;④汽水;⑤二氧化碳;⑥新鮮的空氣;⑦雨水;⑧澄清石灰水;⑨高錳酸鉀受熱完全分解后的剩余固體,其中屬于純凈物的是?��、佗荨?填序號(hào),下同);屬
4��、于混合物的是?��、冖邰堍蔻撷啖帷?���。?
易錯(cuò)點(diǎn)4 物質(zhì)的燃燒
5.下列有關(guān)燃燒現(xiàn)象的描述正確的是(C)
A.木炭在空氣中充分燃燒生成二氧化碳
B.鐵絲在空氣中燃燒火星四射
C.硫在空氣中燃燒生成有刺激性氣味的氣體
D.紅磷在空氣中燃燒產(chǎn)生大量白霧
【解析】A項(xiàng),“生成二氧化碳”的描述不屬于現(xiàn)象;B項(xiàng),鐵絲在空氣中不能燃燒;D項(xiàng),紅磷在空氣中燃燒產(chǎn)生大量白煙��。
易錯(cuò)點(diǎn)5 化合反應(yīng)與氧化反應(yīng)的區(qū)分
6.下列說(shuō)法中正確的是(A)
A.物質(zhì)與氧發(fā)生的化學(xué)反應(yīng)叫氧化反應(yīng)
B.氧化反應(yīng)一定是化合反應(yīng)
C.物質(zhì)在空氣中燃燒,實(shí)質(zhì)上是與空氣中的氧氣發(fā)生化合反應(yīng)
D.石蠟的燃燒既是氧化反應(yīng)
5�����、又是化合反應(yīng)
易錯(cuò)點(diǎn)6 催化劑
7.二氧化錳可用作過(guò)氧化氫分解的催化劑,下列關(guān)于該反應(yīng)中二氧化錳的說(shuō)法正確的是(D)
A.反應(yīng)后其質(zhì)量減小
B.反應(yīng)后其化學(xué)性質(zhì)發(fā)生了變化
C.能使生成的氧氣質(zhì)量增加
D.能改變過(guò)氧化氫分解的速率
8.研究性學(xué)習(xí)小組選擇“過(guò)氧化氫分解生成氧氣的快慢與什么因素有關(guān)”的課題進(jìn)行探究,以下是他們探究的主要過(guò)程����。
【提出猜想】過(guò)氧化氫分解生成氧氣的快慢與催化劑的種類有關(guān)。
【實(shí)驗(yàn)方案】常溫下,取兩份體積相同���、濃度相同的過(guò)氧化氫溶液,分別加入二氧化錳和紅磚粉末,測(cè)定各收集一瓶(體積相同)氧氣所需要的時(shí)間�。
【進(jìn)行實(shí)驗(yàn)】實(shí)驗(yàn)裝置如圖所示,組裝好實(shí)驗(yàn)裝置后
6�、,首先要 檢查裝置的氣密性 ,再將分液漏斗中的液體加入錐形瓶中,立即收集一瓶氣體,此實(shí)驗(yàn)中宜采用的收集氣體的方法是 排水法 。?
【實(shí)驗(yàn)記錄】
實(shí)驗(yàn)編號(hào)
①
②
反應(yīng)物
5%過(guò)氧化氫溶液50 g
5%過(guò)氧化氫溶液50 g
催化劑
紅磚粉末
1 g二氧化錳
收集氣體
所需時(shí)間
165 s
46 s
實(shí)驗(yàn)①中加入紅磚粉末的質(zhì)量是 1 g��。?
【得出結(jié)論】該探究過(guò)程得出的結(jié)論是 相同條件下,過(guò)氧化氫分解生成氧氣的快慢與催化劑的種類有關(guān) ��。?
【反思】過(guò)氧化氫在常溫下分解緩慢,加入二氧化錳或紅磚粉末后反應(yīng)明顯加快,若要證明二氧化錳和紅磚粉末是否為該反應(yīng)的催化劑
7���、,還需要增加實(shí)驗(yàn)來(lái)驗(yàn)證它們?cè)诨瘜W(xué)反應(yīng)前后的 質(zhì)量 和 化學(xué)性質(zhì) 是否改變����。?
過(guò)氧化氫分解生成氧氣的快慢還與哪些因素有關(guān)?請(qǐng)你幫助他們繼續(xù)探究(只要求提出假設(shè)和實(shí)驗(yàn)方案)�。
【假設(shè)】 過(guò)氧化氫分解生成氧氣的快慢與過(guò)氧化氫溶液的濃度有關(guān) 。?
【實(shí)驗(yàn)方案】 常溫下,取兩份體積相同�����、濃度分別為5%�����、10%的過(guò)氧化氫溶液,分別加入相同質(zhì)量的二氧化錳,測(cè)定各收集一瓶(體積相同)氧氣所需要的時(shí)間(合理即可) �。?
易錯(cuò)點(diǎn)7 氧氣的實(shí)驗(yàn)室制取
9.某同學(xué)在制取氧氣時(shí),試管炸裂了,造成試管炸裂的原因可能是下列中的(D)
①?zèng)]有給試管均勻預(yù)熱
②試管外壁有水滴
③試管口沒(méi)有略向下傾斜
④加熱
8、時(shí)試管與燈芯接觸
⑤收集完畢,先撤去酒精燈
A.只有①③ B.只有①③⑤
C.只有①③④⑤ D.①②③④⑤
10.化學(xué)是一門以實(shí)驗(yàn)為基礎(chǔ)的科學(xué),某?�;瘜W(xué)興趣小組用如圖裝置完成實(shí)驗(yàn),請(qǐng)根據(jù)要求回答:
(1)寫出儀器a的名稱: 錐形瓶 �。?
(2)實(shí)驗(yàn)室若要用過(guò)氧化氫溶液制取氧氣,應(yīng)選擇的發(fā)生裝置是 B (填字母序號(hào),下同),收集裝置是 C(或E) 。?
(3)用高錳酸鉀制取氧氣時(shí),要在靠近試管口的部位放一團(tuán)棉花,其目的是 防止高錳酸鉀粉末進(jìn)入導(dǎo)管,堵塞導(dǎo)管 ��。停止加熱時(shí),要先把導(dǎo)管移出水面,后熄滅酒精燈的原因是 防止水槽中的水倒流回試管使試管炸裂 �����。?
11.某化學(xué)興趣小組的
9�����、同學(xué)在對(duì)氧氣性質(zhì)進(jìn)行研究時(shí),設(shè)計(jì)了如下實(shí)驗(yàn)過(guò)程:
(1)利用如圖裝置收集氧氣時(shí),瓶?jī)?nèi)裝滿水,氣體由 b (填“a”或“b”)端通入,之所以能用該方法收集氧氣,是因?yàn)檠鯕狻〔灰兹苡谒也慌c水反應(yīng) 。?
(2)在實(shí)驗(yàn)探究的過(guò)程中,某同學(xué)提出:能使帶火星的木條復(fù)燃所需氧氣的最低體積分?jǐn)?shù)是多少?于是他們準(zhǔn)備用不同體積分?jǐn)?shù)的氧氣來(lái)進(jìn)行實(shí)驗(yàn)����。用排水法收集不同體積分?jǐn)?shù)氧氣的操作是 用集氣瓶分別盛裝不同體積的水,然后用排水法收集氣體,即可收集到各體積分?jǐn)?shù)不同的氧氣 。?
(3)通過(guò)反復(fù)實(shí)驗(yàn),得出最終的實(shí)驗(yàn)現(xiàn)象如表所示(數(shù)據(jù)為體積分?jǐn)?shù)):
1號(hào)瓶(收集
34%的氧氣)
2號(hào)瓶(收集
35%的氧氣)
3號(hào)瓶(收集
36%的氧氣)
4號(hào)瓶(收集
37%的氧氣)
不復(fù)燃
不復(fù)燃,但很亮
很亮,復(fù)燃
立即復(fù)燃
這時(shí)一位同學(xué)脫口而出:氧氣體積約占36%就是使帶火星的木條復(fù)燃的最低體積分?jǐn)?shù)��。而其他同學(xué)立即反對(duì),你的觀點(diǎn)是 反對(duì) (填“贊成”或“反對(duì)”),理由是 該集氣瓶中還有體積分?jǐn)?shù)為64%的空氣,空氣中也有氧氣 ���。?
你認(rèn)為能使帶火星的木條復(fù)燃所需氧氣的最低體積分?jǐn)?shù)是 49% (取整數(shù))���。?
4
 2018年秋九年級(jí)化學(xué)上冊(cè) 第二單元 我們周圍的空氣易錯(cuò)強(qiáng)化練 (新版)新人教版
2018年秋九年級(jí)化學(xué)上冊(cè) 第二單元 我們周圍的空氣易錯(cuò)強(qiáng)化練 (新版)新人教版