《精修版高考化學(xué)大一輪復(fù)習(xí)【40】化學(xué)與工農(nóng)業(yè)生產(chǎn)題組訓(xùn)練含答案》由會(huì)員分享�����,可在線閱讀���,更多相關(guān)《精修版高考化學(xué)大一輪復(fù)習(xí)【40】化學(xué)與工農(nóng)業(yè)生產(chǎn)題組訓(xùn)練含答案(4頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索��。
1�����、精品文檔?高考化學(xué)
高考化學(xué)大一輪復(fù)習(xí) 13.40 化學(xué)與工農(nóng)業(yè)生產(chǎn)題組訓(xùn)練
遞進(jìn)題組 提升素養(yǎng)
最有價(jià)值 備考訓(xùn)練
題組一 重要的化工生產(chǎn)
1.下列化工生產(chǎn)中不涉及氧化還原反應(yīng)的是( )
A.工業(yè)合成NH3 B.接觸法制H2SO4
C.氯堿工業(yè) D.聯(lián)合制堿
解析:聯(lián)合制堿��,未涉及到元素化合價(jià)變化���。
答案:D
2.在NH3����、H2SO4的工業(yè)生產(chǎn)中�,具有的共同特點(diǎn)是( )
A.使用H2作原料 B.使用吸收塔設(shè)備
C.使用催化劑 D.使用尾氣吸收裝置
答案:D
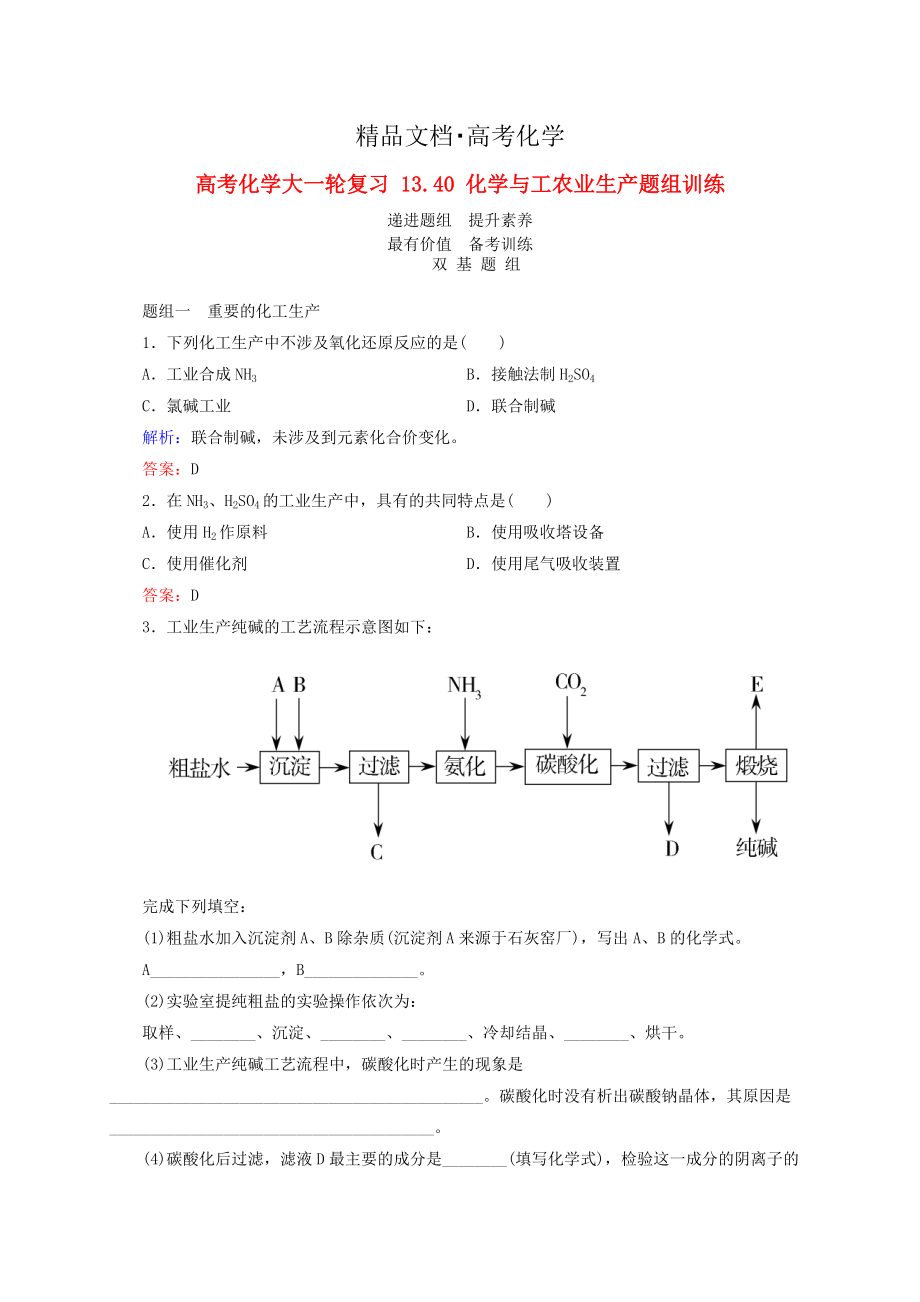
3.工業(yè)生產(chǎn)純堿的工藝流程示意圖如下:
完成下列填空:
(1)粗鹽水加入
2、沉淀劑A���、B除雜質(zhì)(沉淀劑A來(lái)源于石灰窯廠),寫(xiě)出A�����、B的化學(xué)式����。
A________________,B______________�。
(2)實(shí)驗(yàn)室提純粗鹽的實(shí)驗(yàn)操作依次為:
取樣、________��、沉淀�����、________、________���、冷卻結(jié)晶�����、________���、烘干。
(3)工業(yè)生產(chǎn)純堿工藝流程中����,碳酸化時(shí)產(chǎn)生的現(xiàn)象是______________________________________________。碳酸化時(shí)沒(méi)有析出碳酸鈉晶體��,其原因是________________________________________���。
(4)碳酸化后過(guò)濾����,濾液D最主要的成分是___
3、_____(填寫(xiě)化學(xué)式)�����,檢驗(yàn)這一成分的陰離子的具體方法是:_________________________����。
(5)氨堿法流程中氨是循環(huán)使用的,為此�����,濾液D加入石灰水產(chǎn)生氨���。加石灰水后所發(fā)生的反應(yīng)的離子方程式為:___________________�����。濾液D加石灰水前先要加熱,原因是___________________________________����。
(6)產(chǎn)品純堿中含有碳酸氫鈉。如果用加熱分解的方法測(cè)定純堿中碳酸氫鈉的質(zhì)量分?jǐn)?shù)����,純堿中碳酸氫鈉的質(zhì)量分?jǐn)?shù)可表示為:________________________________________________(注明你的表達(dá)式中所用的
4����、有關(guān)符號(hào)的含義)���。
解析:此題考查了物質(zhì)的提純�、化學(xué)實(shí)驗(yàn)基本操作��、實(shí)驗(yàn)結(jié)果的處理等知識(shí)��。
(1)沉淀劑A來(lái)源于石灰窯�����,說(shuō)明其是生石灰或熟石灰���;粗鹽中的鎂離子和鈣離子一般用碳酸鈉除去��;
(2)實(shí)驗(yàn)室提純粗鹽的整個(gè)操作過(guò)程為:取樣��、溶解�����、沉淀��、過(guò)濾���、蒸發(fā)�����、冷卻結(jié)晶�、過(guò)濾�、烘干;
(3)純堿生產(chǎn)中碳酸化時(shí)����,會(huì)看到溶液中析出晶體,析出的晶體不是碳酸鈉晶體�,這是由于碳酸鈉的溶解度大于碳酸氫鈉;
(4)根據(jù)操作過(guò)程���,碳酸化后溶液中主要是NH4Cl;檢驗(yàn)其中的氯離子時(shí)���,要經(jīng)過(guò)取樣�,加硝酸酸化,加硝酸銀溶液有白色沉淀產(chǎn)生�����,則該陰離子是氯離子���;
(5)濾液中主要含有的是氯化銨����,其和石灰水反應(yīng)時(shí):NH
5����、+OH-===NH3↑+H2O;由于濾液中還含有一定量的碳酸氫鈉��,故加石灰水前先加熱�,是為防止加石灰水時(shí)產(chǎn)生碳酸鈣沉淀;
(6)假設(shè)加熱前純堿的質(zhì)量為m1��,加熱后的質(zhì)量為m2�����,則加熱損失的質(zhì)量為:m1-m2���,純堿中碳酸氫鈉的質(zhì)量為:
84(m1-m2)/ 31��;故純堿中含有碳酸氫鈉的質(zhì)量分?jǐn)?shù)為:ω(NaHCO3)=�����。
答案:(1)Ca(OH)2或CaO Na2CO3
(2)溶解 過(guò)濾 蒸發(fā) 過(guò)濾
(3)有晶體析出(或出現(xiàn)渾濁) 碳酸鈉溶解度比碳酸氫鈉大
(4)NH4Cl 取樣�����,加硝酸酸化�,加硝酸銀溶液,有白色沉淀產(chǎn)生��,則該陰離子是氯離子
(5)���、(6)見(jiàn)解析���。
題組二 化學(xué)與技
6、術(shù)的發(fā)展
4.某工廠用CaSO4�、NH3、H2O���、CO2制備(NH4)2SO4���,其工藝流程如圖所示,下列推斷不合理的是( )
A.直接蒸干濾液得到純凈的(NH4)2SO4
B.生成1 mol (NH4)2SO4至少消耗2 mol NH3
C.CO2可被循環(huán)使用
D.往甲中通入CO2有利于(NH4)2SO4生成
解析:因NH受熱水解加劇����,逸出NH3,最后得不到純凈的(NH4)2SO4��,A項(xiàng)錯(cuò)誤����;由元素守恒可判斷B項(xiàng)正確;從流程圖中可看出��,反應(yīng)過(guò)程中需用CO2���,而CaCO3煅燒過(guò)程中產(chǎn)生CO2����,因此CO2可循環(huán)使用���,C項(xiàng)正確�;甲中含有足量的NH3����,通入CO2���,生成(NH4)2CO
7、3�����,有利于生成(NH4)2SO4����,D項(xiàng)正確。
答案:A
5.普鈣是目前使用最廣泛的磷肥�,其主要成分是( )
A.Ca5(PO4)3F
B.Ca(H2PO4)2H2O和CaSO4
C.Ca3(PO4)2和CaHPO4
D.CaHPO4和Ca(H2PO4)2
解析:普鈣的主要成分是Ca(H2PO4)2H2O和CaSO4。
答案:B
[2012海南高考]合成氨的流程示意圖如下:
回答下列問(wèn)題:
(1)工業(yè)合成氨的原料是氮?dú)夂蜌錃?��。氮?dú)馐菑目諝庵蟹蛛x出來(lái)的�����,通常使用的兩種分離方法是________________________���,____________________
8、____����;氫氣的來(lái)源是水和碳?xì)浠衔?,?xiě)出分別采用煤和天然氣為原料制取氫氣的化學(xué)反應(yīng)方程式________________________�,________________________��;
(2)設(shè)備A中含有電加熱器�,觸媒和熱交換器,設(shè)備A的名稱(chēng)是________________________����,其中發(fā)生的化學(xué)反應(yīng)方程式為_(kāi)_______________________;
(3)設(shè)備B的名稱(chēng)是__________________________�����,其中m和n是兩個(gè)通水口��,入水口是________________________(填“m”或“n”)���。不宜從相反方向通水的原因是________
9�、________________�����;
(4)設(shè)備C的作用是________________________;
(5)在原料氣制備過(guò)程中混有的CO對(duì)催化劑有毒害作用����,欲除去原料氣中的CO,可通過(guò)如下反應(yīng)來(lái)實(shí)現(xiàn):CO(g)+H2O(g)CO2(g)+H2(g)
已知 1 000 K時(shí)該反應(yīng)的平衡常數(shù)K=0.627���,若要使CO的轉(zhuǎn)化率超過(guò)90%�����,則起始物中c(H2O)∶c(CO)不低于________________�。
解析:(1)提取空氣中的氮?dú)饪捎梦锢矸椒ǚ蛛x液態(tài)空氣法�,也可以用化學(xué)方法反應(yīng)掉其中的氧氣。
(3)冷凝分離產(chǎn)品設(shè)備為冷凝器����,入水口應(yīng)該在下面,因逆向冷凝效果好�����。
(4)
10�、分離器是氣—液分離專(zhuān)用設(shè)備。
(5)以轉(zhuǎn)化率為90%為基準(zhǔn)計(jì)算,用平衡常數(shù)求水與一氧化碳濃度比���。
設(shè)CO��、H2O起始濃度分別為x��、y
CO(g)+H2O(g)CO2(g)+H2O(g)
c起 x y 0 0
c變 0.9x 0.9x 0.9x 0.9x
c平 0.1x y-0.9x 0.9x 0.9x
K==0.627
y∶x=13.8�����。只要水更多一些,則轉(zhuǎn)化率會(huì)超過(guò)90%�����。
答案:(1)液化����、分餾 與碳反應(yīng)后除去CO2
C+H2OCO+H2
CH4+H2OCO+3H2
(2)合成(氨)塔
N2+3H22NH3
(3)冷卻塔(或冷凝器) n 高溫氣體由冷卻塔的上端進(jìn)入,冷卻水從下端進(jìn)入�����,逆向冷卻效果好
(4)將液氨與未反應(yīng)的原料氣分離 (5)13.8
 精修版高考化學(xué)大一輪復(fù)習(xí)【40】化學(xué)與工農(nóng)業(yè)生產(chǎn)題組訓(xùn)練含答案
精修版高考化學(xué)大一輪復(fù)習(xí)【40】化學(xué)與工農(nóng)業(yè)生產(chǎn)題組訓(xùn)練含答案